Por Ingrid Ferreira Costa
Mariana Baptistão
O avanço tecnológico das técnicas químicas possibilitou que muitas perguntas técnico- científicas fossem respondidas, principalmente, porque as análises químicas clássicas demandavam uma quantidade razoável de amostra para chegar em um resultado conclusivo. Em contrapartida, os instrumentos de análise instrumental aumentaram exponencialmente sua sensibilidade, e por isso, começaram a demandar um cuidado maior no preparo das amostras. A maioria das amostras encontradas em laboratórios que realizam análises cromatográficas não estão numa forma que possibilite uma análise direta, ou seja, é necessário alguma forma de preparação para quase todas as amostras. Esse preparo pode ser simples como uma diluição ou mais complexo, como quando envolve diversas etapas até obter um extrato final adequado. O ciclo ou fluxo analítico, conforme mostrado na Figura 1, engloba todos as etapas de trabalho, desde aquelas iniciais como a coleta e amostragem, até a análise instrumental e tratamento estatístico dos dados. Uma das etapas mais importantes desse ciclo é o preparo de amostras, apesar de nem sempre receber a devida importância quando comparado a seleção da
técnica analítica ou ao tratamento de dados.
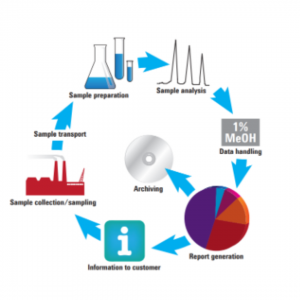
Figura 1. Principais Etapas do Ciclo Analítico. Da esquerda para a direita: coleta/amostragem, transporte das amostras, preparo das amostras, análise das amostras, tratamento de dados, geração de relatório (arquivo) e informação ao cliente final.
Fonte: Majors, 2013.
Ainda avaliando este cenário, deve-se considerar que muitos laboratórios ainda empregam métodos clássicos que são morosos, requerem uma quantidade significativas de solventes,
vidrarias (que podem não ser passíveis de calibração) e com isso a qualidade na entrega dos resultados pode ser questionavél e ainda pode criar problemas de segurança e aumento dos custos no laboratório. Considerando essa temática, nesse artigo será discutido as principais técnicas de preparo de amostras para cromatografia que abrangem as três subáreas: filtração, purificação e extração. As técnicas variam em complexidade de execução, capacidade de limpeza da amostra e custo operacional. Independente disso, o intuito de todas essas técnicas é fornecer uma amostra preparada que:
1. Seja livre de interferentes, o máximo possível;
2. Evite danificar a coluna cromatográfica e o instrumento;
3. Compatível com a técnica de análise.
Um dos processos mais simples de preparo é a filtração das amostras. Esse procedimento é realizado utilizando um filtro de papel ou filtro de seringa, e tem como propósito remover os particulados que podem afetar o sistema cromatográfico com entupimentos, causar danos na cromatografia (por exemplo perda de resolução ou variação no tempo de retenção) e ainda a diminuição no tempo de vida útil da coluna. Esse processo amplamente aplicado em laboratórios farmacêuticos, e também, na finalização de outros métodos de preparo de amostras que são multietapas, mas quem ainda podem conter particulados no extrato final. A seleção do filtro de seringa correto envolve avaliar a compatibilidade química da
membrana com o solvente da amostra, o volume de amostra a ser filtrado com o tamanho do filtro adequado e o tamanho de partícula da coluna analítica para definição da porosidade. Algumas situações conhecidas como a membrana PES (polietersulfona) para amostras biológicas e a RC (celulose regenerada) para PFAS (substâncias perfluoroalquídicas) podem ser citadas, embora ainda existam diversas opções e sempre testes preliminares de recuperação no filtro são recomendados. Atualmente, o formato mais difundido do filtro é aquele para acoplamento a seringa. Mas existe a possibilidade de filtrar amostra com maior conveniência usando vials com filtro embutido na tampa, para realização desse processo dentro do vial – uma facilidade que vai dispensar o uso da seringa e que com isso manterá a eficiência do procedimento mas com menos etapas,
diminuindo as chances de contaminação. A desvantagem nesse caso é a menor disponibilidade de membranas nesse formato.
Ainda dentro da área de filtração, existem procedimentos mais seletivos que, além da remoção do particulado, podem agregar a remoção de classes de compostos interferentes, como as proteínas e os lipídios. Eles são interferentes comuns em amostras biológicas e de alimentos, e quando não são eliminados da forma correta geralmente acumulam dentro da fonte de íons do LC-MS ou GC-MS bem como na entrada da coluna analítica, afetando a sensibilidade e robustez dos métodos. Uma forma moderna de realizar essa remoção é a partir de placas filtrantes de 96- posições que contém fase estacionária. Uma vez desenvolvidos e otimizados com os solventes e quantidades adequadas, esses protocolos promoverão simultaneamente a remoção de proteínas e/ou lipídios juntamente com o particulado. Os métodos em placas filtrantes são conhecidos por economizar tempo e fornecer maior eficiência ao preparo frente aos procedimentos clássicos para tais fins, como por exemplo a precipitação de proteínas. Uma outra vantagem dessas placas é a alta produtividade, ideal para laboratórios com alta demanda de análises por dia e também a possibilidade de automatização do protocolo com pipetadores automáticos – algo impensável com os métodos clássicos. Aplicações como Análise de Vitaminas, Quantificação de Hormônios e Identificação de Drogas em matrizes diversas podem ser citadas como algumas das indicadas para esse tipo de preparo de amostras. Dentro da área de purificação, abordaremos a técnica de extração líquida, sendo a mais popular delas a extração líquido-líquido (LLE). A LLE clássica é baseada na miscibilidade dos compostos com os meios orgânico e aquoso para a extração, e para atingir uma boa recuperação é comum utilizar grandes volumes de solvente orgânico, muitas vezes solventes perigosos, e como consequência os procedimentos são conhecidos por serem morosos e de difícil operação.
Recentemente, houve grande interesse em miniaturização de métodos analíticos que resultam em economia de solvente, amostra e de tempo, e sendo assim, novos métodos LLE
miniaturizados já foram reportados e comparados com técnicas clássicas, sendo que essas abordagens se mostraram mais eficientes e fácil automatização. Em contrapartida, uma outra forma moderna de endereçar as dificuldades já mencionadas e outras (como formação de emulsão e variação de resultados analista-a-analista, por exemplo) da extração líquido-líquido é optar pela extração sólido-líquido (SLE). Com a SLE não há agitação vigorosa no funil de separação, e, portanto, as emulsões não serão formadas. Além disso, a partição é extremamente eficiente entre a fase líquida e o suporte sólido levando a procedimentos mais reprodutíveis, pois a dependência do tipo de agitação, tempo de agitação e visualização da separação de fases de cada analista deixam de existir. O suporte sólido da SLE pode ser baseado em terra diatomácea ou materiais sintéticos, que nesse processo tem a função de adsorver todo o conteúdo da amostra, e depois com o solvente orgânico adequado, analitos são eluídos. A lista de possibilidades de aplicação é vasta, mas vale citar especialmente os segmentos de cosméticos, alimentícios e da pesquisa clínica. Limitações existem para amostras sólidas e/ou analitos de alta polaridade. QuEChERS, acrônimo do inglês (Quick, Easy, Cheap, Effective, Rugged and Safe) é uma técnica que tem recebido grande destaque por ter sido rapidamente incorporada nos protocolos de laboratórios em todo o mundo. Sua metodologia é amplamente utilizada para a análise de resíduos de pesticidas e contaminantes orgânicos em amostras de alimentos. O procedimento consiste em duas etapas rápidas e muito simples de extração e limpeza. Quando comparado com métodos clássicos, esse procedimento reduz uso de solventes caros e perigosos, necessita de
uma quantidade de amostra inicial menor e faz uso de itens simples do laboratório (centrífuga, pipetas e balança analítica). Por fim, com a amostra preparada, o procedimento é amigável com várias técnicas e a análise costuma ser realizada por GC-MS/MS e/ou LC-MS/MS. Aplicações como determinação de resíduos de pesticidas, micotoxinas e drogas veterinárias são algumas das que mais utilizam a técnica de QuEChERS como preparo de amostra. Para aquelas aplicações em que é oportuno realizar a pré-concentração de analitos ou para maior seletividade no procedimento de preparo de amostras por complexidade das matrizes, a extração em fase sólida (SPE) é uma das técnicas mais utilizadas nos laboratórios, principalmente, pela versatilidade, fácil automatização, ausência de emulsão e alta remoção de interferentes. A técnica consiste em utilizar cartuchos com sorventes que atuam com diferentes mecanismos de extração (polar, apolar, troca iônica, etc), de forma que com os solventes adequados é possível fracionar a amostra, eliminando interferentes e eluindor os analitos em etapas distintas. No desenvolvimento e otimização do método é importante verificar as características químicas dos analitos, a compatibilidade química da amostra e dos solventes aplicados em cada etapa. Por conta da disponibilidade de diferentes sorventes a técnica tem alta aplicabilidade em todos os segmentos, sendo de maior destaque o ambiental e alimentício. A extração e concentração de resíduos de contaminantes, que se encontram em níveis muito baixos, em água e efluentes é uma das aplicações com grande demanda para a técnica. Quando os analitos tem um certo grau de volatilidade, a microextração em fase sólida (SPME) é aplicada, explorando não apenas um sorvente/fase extratora mas também a temperatura, para melhor recuperar os analitos. Um pouco diferente do SPE, a fase extratora não encontra-se num cartucho e sim numa fibra com espessura conhecida de fase recoberta. Os métodos permitem que a amostra entre em contato direto com a fibra ou deixam um espaço disponível entre as fases (chamado de headspace) por um determinado período de tempo até que seja estabelecido um equilíbrio e com isso os analitos consigam adsorver na superfície da fase extratora. O desenvolvimento e otimização desses métodos envolve o entedimento e avaliação de parâmetros como o pH, temperatura, tempo de extração, agitação, entre outros.
Aplicações como resíduos de solvente em matéria-prima, surfactantes e impurezas em polímeros tipicamente são feitas por SPME. Com as informações e aplicações apresentadas, verifica-se a grande aplicabilidade das técnicas de preparo de amostra em vários segmentos de mercado. De forma geral, a necessidade de uma técnica mais seletiva de preparo de amostra tende a aumentar proporcionalmente com o aumento da complexidade da amostra a ser analisada, porém outras necessidades do método analítico como sensibilidade e seletividade devem ser contabilizadas. Não há uma técnica de preparo de amostras ideal para todas as aplicações, e essa escolha sempre deve estar atrelada
às perguntas técnico-científicas definidas no início – o preparo de amostra precisa ser bom o suficiente para responder a essas perguntas.
REFERÊNCIAS
MAJORS, Ron E.; Sample Preparation Fundamentals for Chromatography. Wilmington, DE. Agilent Technologies, Inc., 2013. 364 p. https://www.agilent.com/cs/library/primers/Public/5991-3326EN_SPHB.pdf
PRESTES, Osmar D.; FRIGGI, Caroline A.; ADAIME, Martha B.; ZANELLA, Renato. QuEChERS: um método moderno de preparo de amostra para determinação multirresíduo de pesticidas em alimentos por métodos cromatográficos acoplados à espectrometria de massas. Química Nova, [S.L.], v. 32, n. 6, p. 1620-1634, 2009. FapUNIFESP (SciELO). http://dx.doi.org/10.1590/s0100-40422009000600046.
VALENTE, Antonio Luiz Pires; AUGUSTO, Fabio. Microextração por fase sólida. Quím. Nova [online], v. 23, n. 4, p. 523-530, 2000. ISSN 1678-7064. https://doi.org/10.1590/S0100-40422000000400016.
CUNHA, Isabela Cristina Matos. Desenvolvimento e Validação de um Método para Determinação de Formaldeído em Esmaltes Utilizando QuERChES/SPE e GC/MS. 2016. 96 f. Tese (Doutorado) – Programa de Pós Graduação em Química, Universidade Federal de Ouro Preto, Ouro Preto, 2016.
Sobre as Autoras
Ingrid Ferreira Costa – Contato: cif.ingrid@gmail.com
Mestranda em Ciências Farmacêuticas (UNIFESP) atuando na linha de pesquisa de Desenvolvimento e Inovação Farmacêutica focado no estudo metabolômico de microrganismos e plantas medicinais. MBA em Marketing Estratégico Digital. Especialista em Growth Hacking. Bacharel em Química com Atribuições Tecnológicas (UNIFESP e FASB). CEO da Biochemie, Empreendedora Científica, Especialista em P&D, sobretudo, em executar investigações analíticas e know-how em desenvolver novas metodologias analíticas.
Mariana Baptistão – mariana.baptistao@agilent.com
Bacharel em Química e Mestre em Química Analitica pela Universidade Estadual de Campinas (UNICAMP). Atua como Cientista de Aplicação de Consumíveis desde 2014 na Agilent Technologies do Brasil, com experiência em desenvolvimento de métodos analíticos em cromatografia e métodos de preparo de amostras para cromatografia.
Leia nossa revista digital disponível AQUI








