A técnica da Cromatografia a gás acoplada a Espectrometria de massas abre novos caminhos para elucidar a estrutura da matéria. Esta técnica é denominada técnica hibrida já que cada uma das suas partes realiza um determinado processo analítico, a cromatografia a gás em inglês GC “Gas Chromatography”, realiza a separação dos componentes de uma mistura gasosa a ser analisada e a espectrometria de massas, em inglês MS “Mass Spectrometry”, realiza a identificação dos componentes químicos gasosos separados pelo GC. Desta forma o analisador GC/MS (Figura 1) funciona no modo Tandem, onde os compostos químicos precursores de uma mistura gasosa são separados pelo GC e logo detectados e quantificados em seus produtos, pelo MS. Quem trabalha com cromatografia denomina o MS como detector num sistema GC/MS, mas quem trabalha com MS denomina o GC como sistema de introdução de amostra, cabe ao leitor decidir a preferencia.
O GC/MS aumentou o poder analítico enormemente na química. O GC acoplado com outro detector, não sendo o MS, tal como o da Ionização de Chama (Flame Ionization Detector – FID) e conhecido como GC/FID, realiza análises de compostos químicos somente quando o analisador é calibrado anteriormente com padrões previamente estabelecidos e conhecidos. Por outro lado o MS discrimina os analitos por meio de sua razão massa/carga (m/z), mas tem a contribuição no seu espectro de fracionamentos moleculares além das contribuições isotópicas, facilitando a identificação do analito por meio do espectro de massas (Figura 2).
A cromatografia a gás é definida como um método físico-químico de separação dos componentes de uma mistura, que são distribuídas em duas fases intimamente ligadas: fase estacionária contida na coluna cromatográfica e fase móvel, denominado gás de arraste que a percorre, contendo os analitos a serem separados. Durante a passagem da fase móvel sobre a estacionária, os componentes do analito são distribuídos e retidos na fase estacionária conforme a sua afinidade físico-química, sendo logo eluídos seletivamente em direção ao analisador, resultando em migrações diferenciais para cada analito, cuja unidade é o Tempo de Retenção – TR, medida em minutos.
As principais partes de um cromatógrafo são (Figura 1): o injetor, coluna e detector, neste caso o MS. A amostra líquida, gasosa ou sólida, contendo os analítos é introduzida no injetor. O uso de temperatura no sistema de injeção favorece a vaporização da amostra, para amostras líquidas ou sólidas, sendo introdução direta para amostras gasosas. Os analítos no estado gasoso são carregados pelo gás de arrastre para a coluna. A coluna capilar é constituída por sílica fundida de diâmetro interno de 0,1 mm com fase estacionária interna, polar ou apolar, de acordo afinidade dos analistos. A coluna fica condicionada num forno resistivo programável. A programação da temperatura na coluna contribui para separação dos analitos devido as suas características, tais como, volatilidade, ponto de ebulição, peso molecular e estabilidade térmica. Cada espécie separada apresentará diferente tempo de retenção (RT), que ao chegar ao fim da coluna, segue para o detector.
O detector dos analítos é o Espectrômetro de massas. O MS esta constituído de fonte de íons, analisador e detector (Figura 1). Quando uma das substâncias emerge da coluna e ingressa no Espectrômetro de massas, através da linha de transferência, a mesma interage com elétrons acelerados emanados por um filamento, gerando íons do analíto na fonte de íons. Nesse local os analitos na forma de íons são fragmentados de acordo a suas ligações químicas (Figura 2) seguindo um padrão de fragmentação constante e único para uma dada energia de ionização que geralmente é de 70 eV, tal como uma impressão digital para cada molécula do analíto em estudo, facilitando a construção de um banco padrão de espectros de massas de interesse, entre estes os padrões da “National Institute of Standards and Technology – NIST”.
Os íons gerados na fonte de íons são acelerados e introduzidos no analisador de quadrupolo, constituído de quatro barras cilíndricas ligadas eletricamente em DC e RF em pares, mas com fases opostas eletronicamente. Dentro deste campo eletromagnético, os íons do analíto sofrem o efeito eletromagnético e são filtrados pelas barras cilíndricas de acordo com sua razão massa/carga (m/z). Somente uma espécie de íons com uma determinada m/z passará através dos quadrupolos sem colidir com as barras. Finalmente, estes íons são detectados e contados pelo multiplicador de elétrons, denominado detector. Desta forma discretizando massas de 1 a 1090 m/z, em intervalos de tempo de micro segundos é construído um espectro de massas em menos que um segundo. O número de íons de cada espectro de massas gerado é utilizado para construir o cromatograma por meio de um “software”. Assim, todo GC/MS gera duas informações para o analista químico, um cromatograma e milhares de espectros de massas. O cromatograma (Figura 2a) apresenta a intensidade total dos íons detectados “Total Ion Current – TIC” (eixo y) em função do Tempo de Retenção em minutos da eluição de cada analito (eixo x). Os espectros de massas apresentam as análises dos compostos químicos presentes na eluição a cada segundo, com uma vantagem, podendo ser comparados com o banco de dados da NIST para uma possível detecção do analito desejado. Todo espectro de massas (Figura 2b) apresenta a intensidade relativa dos íons fragmentos e do íon molécula de cada analito (eixo y) em função da razão m/z (eixo x) de cada fragmento detectado.
A união do GC/MS demorou a ser descoberta devido as suas peculiaridades intrínsecas, o GC trabalha a pressões positivas, isto é, pressões maiores à atmosférica e o MS a pressões negativas, isto é, vácuo. Como compatibilizar um instrumento que funciona a pressões positivas e outra negativa? Como coletar tantos dados em cada análise realizada? Sendo que a eluição dos analítos gerando um cromatograma, demora em torno de 30 a 60 minutos, armazenando um espectro de massas por segundo isto significa 1800 a 3600 espectros de massas por análise, acarretando a necessidade de Megabytes (MB) de memória no computador.
Para resolver o problema da incompatibilidade de pressões, foi desenvolvida uma bomba de vácuo mais potente, para poder drenar rapidamente o MS. Assim surgiu a bomba de vácuo Turbo-molecular (Figura 1). Além disso, teve que se diminuir o fluxo da fase móvel da coluna cromatográfica atingindo-se até 1 mL/min. Para resolver o problema da coleta de amostras do GC/MS, computadores com maior capacidade de memória são utilizados. O Prof. Peter Atkins no seu livro “What is chemistry?” diz: “O instrumento que transformou a química, assim como transformou a vida nesta última década é o computador. Graças ao computador pode se simular e modelar as novas moléculas sintetizadas, sendo esta nova ciência denominada química computacional”. A mesma é aplicada no analisador GC/MS.
Vários modos de análise no GC/MS são possíveis de serem utilizados. Entre estes: modo “scan mass – SCAN” ou varredura de massas, onde são analisadas todas as massas dos analitos num determinado intervalo de massas. Este modo é utilizado para análise de uma amostra desconhecida. Modo “Selected Ion Monitoring – SIM” onde apenas os íons desejados são monitorados, analisando só uma ou várias espécies iônicas específicas. Este modo é utilizado na análise quantitativa de um ou vários analítos (Figura 2a).
Superados os problemas da gênesis do GC/MS, hoje em dia é um analisador versátil para a análise de compostos químicos especialmente a nível traços. Seus usuários cada dia exploram mais o analisador tornando um instrumento de rotina no laboratório de análises química sendo até utilizados nas explorações extraterrestres pela NASA. Diminuiu seu tamanho, tornando-se um analisador de bancada, comercialmente vendido como “Bench-Top”. Além disso, o seu custo, ficou cada vez mais accessível para os mais humildes laboratórios.
O GC/MS é um método rápido que fornece informações valiosas sobre a análise de produtos naturais usado para analisar misturas orgânicas e bioquímicas complexas, pesticidas e compostos orgânicos voláteis e semivoláteis no meio ambiente. A principal desvantagem do uso do GC/MS é de ser incapaz de analisar compostos não voláteis, polares ou termicamente lábeis, sendo necessária a derivatização para aumentar a volatilidade e a estabilidade térmica desses compostos.
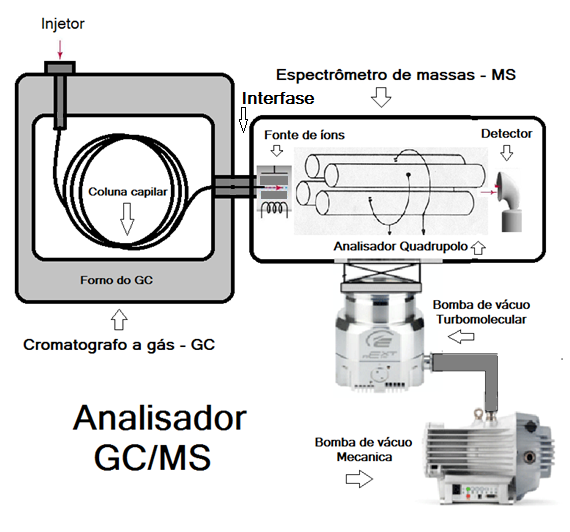
Fonte: Redígolo, 2020
Figura 1: Analisador GC/MS. Constituído de dois compartimentos separados: um contém o GC e outro o MS. O GC está composto por: injetor da amostra, coluna cromatográfica e forno resistivo programável. O MS está formado por: da fonte de íons, analisador de massas quadrupolar e detector de íons. O MS funciona sob alto vácuo obtida por meio de bomba turbomolecular e bomba mecânica de pré-vácuo.
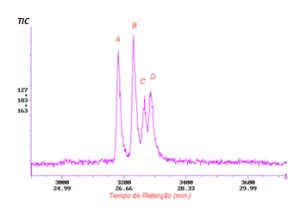
(a)
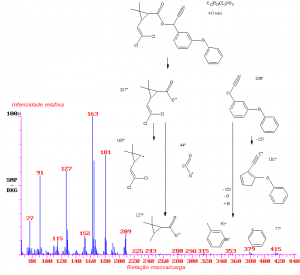
(b)
Fonte: Sassine, 2002
Figura 2: Análise do Piretróide Cipermetrina na matriz leite. (a) Cromatograma da molécula Cipermetrina em modo SIM, monitorando os íons m/z 127, 163 e 181. Assinala-se a presença de quatro diasterónimos cis-1, cis-2, trans-1 e trans-2; A, B, C, D, respectivamente. (b) Espectro de massas da Cipermetrina apresentando o íon molécula m/z 415, altamente fragmentado e seus principais fragmentos m/z 77, 91, 127, 163, 181 com suas respectivas representações iônicas químicas.
Referências bibliográficas
- Sassine, A.; Moura, S.; Léo, V. and Bustillos, O. “Cypermethrin residues determination in the milk of a lactating dairy cow by gas chromatography – Ion Trap mass spectrometry”. of Analytical Toxicology. V.28, 2004.
- Redígolo, M.M.; Costa, I.; Vega, O. “Cadernos de ciência da conservação Volume 1. Tintas brasileiras”. Ed. Scortecci. 1ª Ed. 2020.
- Atkins, P. “What is chemistry”. Oxford University Press. 2013.

*Oscar Vega Bustillos
Pesquisador do Centro de Química e Meio Ambiente CQMA do Instituto de Pesquisas Energéticas e Nucleares IPEN/CNEN-SP
55 11 3133 9343
www.vegascience.blogspot.com.br
< Artigo disponível na íntegra na Revista Analytica Ed 105. >






